濃縮複合ミネラル硅素水とは?
当社の硅素は、SiO3の硅素水であり、特許取得の特別な硅素水です。
このSio3というのが、キーポイントです。
一般的には、ケイ素水が身体に良いと言われていますが、これは間違いです。
ケイ素水とは、兎に角、種類が多く、毒になるケイ素水もありますので注意が必要です。
ケイ素水でも、当社の硅素水は、正真正銘のSio3の特許を取得した硅素水なのです。
硅素とは?

地球上で酸素の次に多い元素(元素記号Si)結晶質(ガラス・水晶など)と非結晶質(水溶性)がある。
近年シリコンとして、半導体に利用。
ドイツでは、硅素が身体に良い事が認知されている。
アメリカ軍では、腐敗防止のために水筒に硅素をいれている。
電磁記録素材として研究。
硅素の利用は世界の常識となっている。
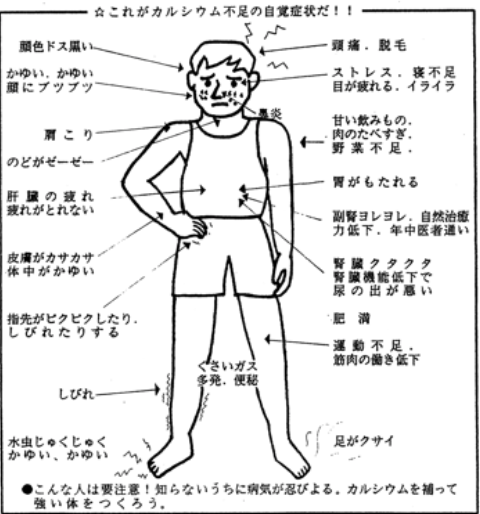
硅素の効果
コラーゲンの生成に関与。
肌・爪・髪の毛などを構成する必須ミネラル。
農薬や添加物などを吸着し体外に排出。
人体における硅素の重要性が、フラミンガム子孫研究結果のより発表。
硅素を体内に入れる事で、恒常性維持機能が改善され、人間が本来持っている免疫機能が改善される。
硅素を用いた実験
乳化実験 油分に硅素水を滴下後、瞬時に乳化。

酸化実験 硅素水に浸した釘は1カ月経過後も錆びない。

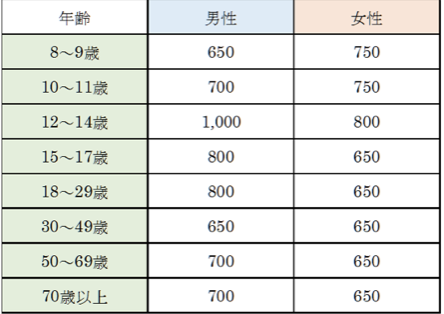
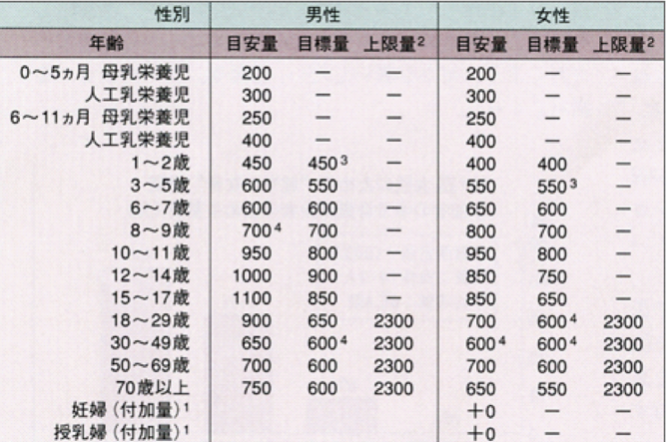
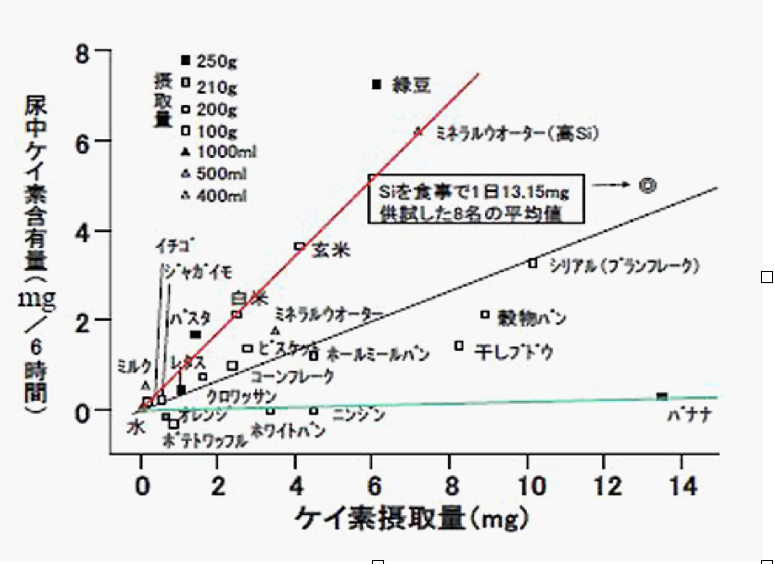
ケイ素摂取量と尿中ケイ素含有量
硅素を特集している記事


肌、髪、骨の健康に効果絶大!?「ケイ素」を上手に摂取する方法
硅素水とソマチットの関係
硅素は、体内ソマチットの栄養源になる。
硅素により、体内環境が、正常化になると、ソマチットが活性化し、増殖する。
当社の進化ソマチットがより効果をアップ!
血清中ケイ素は、経口摂取2時間後にピークになり、腎臓を経由して、6時間内には尿より大部分が排出される。

鹿児島大学でのマウスの臨床試験の結果
特許によると、糖尿病、癌の転移をしなかった効果が認められています。
リウマチ・ヘルニアなどの神経痛、高血圧、脳梗塞、潰瘍、アレルギー、アトピー性皮膚炎、皮膚疾患、喘息などの肺疾患、便秘、火傷、水虫等の改善効果があると考えられています。
さらに、当社のスーパーNEO微粉末ソマチットカルシウムを併用する事で、効果が倍増されます。
山﨑教男先生の特許公報
多孔性球状メタケイ酸コロイド溶液で特許取得特許第4564076号
生命科学関連特許情報
| タイトル: | 特許公報(B2)_多孔性球状メタケイ酸コロイド溶液 |
| 出願番号: | 2008111395 |
| 年次: | 2010 |
| IPC分類: | A61K 33/00,A61K 33/12,A61P 13/12,A61P 3/10,A23L 1/304,A23L 2/52,A23L 2/38,C01B 33/32 |
特許情報キャッシュ
小原 徹 濱田 教男 西園 啓文 JP 4564076 特許公報(B2) 20100806 2008111395 20080422 多孔性球状メタケイ酸コロイド溶液 株式会社ミラクルウォーター 506216350 葛和 清司 100102842 小原 徹 濱田 教男 西園 啓文
本発明は、水溶性のメタケイ酸塩を含有するメタケイ酸塩溶液、該メタケイ酸塩溶液を含有する飲食物、ならびに腎機能障害および糖尿病の予防剤または改善剤に関する。 ケイ酸塩は、土壌等の環境中に広く分布しており、ヒトをはじめとする動物はケイ酸塩を日常的に超微量摂取しており、ヒトはケイ酸塩により何らかの影響を受けていると考えられる。しかし、ケイ酸塩の利用はシリコンウェハー素材等の産業利用等に限られており、ケイ酸塩(SiO32−)の生体への影響、過剰摂取による健康被害の有無等を詳細に検討した研究は少ない。 韓国特許第10−0589952号(特許文献1)は、水晶を高温で焼成し、水溶性のメタケイ酸塩として取り出す方法を記載している。この方法によって得られるメタケイ酸塩は、高い水溶性を有するものの、腎機能または糖尿病に対する効果は報告されておらず、また、ヒトが大量に摂取した場合に胃もたれを起こす等の不都合を生じる。韓国特許第10−0589952号公報 したがって、本発明の目的は、ヒトを含む動物の生体機能に良好に作用するケイ酸塩溶液を提供することにある。 上記目的に鑑み鋭意研究の結果、本発明者らは、メタケイ酸塩をアルカリ性溶液とすることにより、腎機能障害または糖尿病の病状を改善できること、および水溶液の安定性が向上するとともに、摂取した場合の胃もたれ等の不都合を解消できることを見出し、さらに研究を進めた結果、本発明を完成するに至った。 すなわち、本発明は、水溶性のメタケイ酸塩および水を含有し、pHが8~12である、メタケイ酸塩溶液に関する。 また、本発明は、ケイ素酸化鉱物由来のメタケイ酸塩、カルシウムまたはカルシウム塩、およびマグネシウムを含有する複合水溶液から得られる、前記メタケイ酸塩溶液に関する。 さらに、本発明は、メタケイ酸塩をケイ素として10~1000mg/L含有する、前記メタケイ酸塩溶液に関する。 また、本発明は、メタケイ酸塩をケイ素として500~1000mg/L含有する、前記メタケイ酸塩溶液に関する。 さらに、本発明は、メタケイ酸塩をケイ素として10~100mg/L含有する、前記メタケイ酸塩溶液に関する。 また、本発明は、pHが10~12である、前記メタケイ酸塩溶液に関する。 さらに、本発明は、pHが8~9である、前記メタケイ酸塩溶液に関する。 また、本発明は、前記メタケイ酸塩溶液を含有する飲食物に関する。 さらに、本発明は、ミネラル水である、前記飲食物に関する。 また、本発明は、前記メタケイ酸塩溶液を含有する腎機能障害の予防剤または改善剤に関する。 さらに、本発明は、前記メタケイ酸塩溶液を含有する糖尿病の予防剤または改善剤に関する。 本発明によれば、水溶性メタケイ酸塩を飲食物または経口製剤として摂取することにより腎機能障害または糖尿病を改善することができる。また、水溶性メタケイ酸塩を腎機能障害または糖尿病の予防に用いることもできる。さらに、水溶性メタケイ酸塩を含むアルカリ性溶液とすることにより、胃もたれ等の望ましくない作用を防止することができるとともに、水溶液を安定化することができる。特にメタケイ酸塩溶液を濃縮液とすることにより安定性を一層向上させることが可能である。[I]メタケイ酸塩溶液 本発明のメタケイ酸塩溶液は、水溶性のメタケイ酸塩を含有する。水溶性のメタケイ酸塩は水に対し溶解性の高いメタケイ酸塩であれば特に限定されないが、好ましくはケイ素酸化鉱物(水晶、石英等)由来のメタケイ酸塩であり、特に好ましくは、韓国特許第10−0589952号に記載の、水晶を1650℃以上で焼成し、ガス化した後に回収することにより得られるメタケイ酸塩である(製品名:シリポリ,SILIPOLY、韓国エスカム社製)。 メタケイ酸塩の塩の形態は特に限定されず、メタケイ酸ナトリウム、メタケイ酸カリウム等のアルカリ金属塩、メタケイ酸カルシウム、メタケイ酸マグネシウム等のアルカリ土類金属塩、ジアルミノメタケイ酸カルシウム等を用いることができる。 本発明のメタケイ酸塩溶液中のメタケイ酸塩は、ケイ素として10~1000mg/Lの範囲で用いることができる。例えば、メタケイ酸塩溶液をそのまま飲食物(例えば、ミネラル水)または腎機能障害の予防もしくは改善剤または糖尿病の予防もしくは改善剤として用いる場合、メタケイ酸塩溶液中のメタケイ酸塩の濃度は、ケイ素として好ましくは10~100mg/L、より好ましくは20~50mg/Lである。また、メタケイ酸塩溶液を使用時に希釈する濃縮液として用いる場合、メタケイ酸塩溶液中のメタケイ酸塩の濃度は、ケイ素として好ましくは500~1000mg/L、より好ましくは600~800mg/Lである。この場合、使用時にメタケイ酸塩濃縮液を水等で希釈し、例えば、2容量%溶液または5容量%溶液として用いることができる。 本発明のメタケイ酸塩溶液は、pHが8~12のアルカリ性であるとともに、通常コロイド溶液として存在する。このコロイド溶液の走査電子顕微鏡(SEM)測定の結果、繊維状のコロイド粒子が凝集し、多孔性球状コロイド(図1.1)を形成している。これに対し、韓国特許第10−0589952号に記載のメタケイ酸塩溶液は、コロイド溶液が粘菌状コロイド(図1.2)である点で異なる。これは、水溶性メタケイ酸塩の溶解方法の違いにより、コロイド粒子の形成が大きく異なることを示している。 本発明のメタケイ酸塩溶液は、溶液をアルカリ性することにより、メタケイ酸塩が析出する等の安定性の問題を解消するとともに、ヒトが摂取したときの胃もたれ等の問題も解消することができる。さらに、驚くべきことに、本発明者らはアルカリ性のメタケイ酸塩溶液においてヒトの腎機能または糖尿病の病状の改善が見られるのに対し、韓国特許第10−0589952号に記載のメタケイ酸塩溶液においてはこのような効果が見られないという知見を得ている。 本発明のメタケイ酸塩溶液をそのまま飲食物(例えば、ミネラル水)または腎機能障害もしくは糖尿病の予防剤もしくは改善剤として用いる場合、メタケイ酸塩溶液のpHは好ましくは8~9である。また、本発明のメタケイ酸塩溶液を使用時に希釈する濃縮液として用いる場合、メタケイ酸塩溶液のpHは好ましくは10~12である。pHが高い方がメタケイ酸塩溶液の安定性は向上する。 メタケイ酸塩溶液は、pHを適切な範囲に調整するために、pH調整剤を含有してもよい。pH調整剤としては、例えば、Na+、K+、Mg2+、Ca2+、Cl−、SO42−、HCO3−、HPO42−およびPO43−からなる群から選ばれた少なくとも1種のイオンを用いることができる。 本発明のメタケイ酸塩溶液は、本発明の目的を損わない範囲で上記成分以外の他の成分を含有してもよい。 本発明のメタケイ酸塩溶液は、好ましくはケイ素酸化鉱物由来のメタケイ酸塩、カルシウムまたはカルシウム塩、およびマグネシウムを水に加え、煮沸、冷却等の処理を施すことによって得られる。特に好ましくはメタケイ酸塩[シリポリ;メタケイ酸ナトリウム10水和物(Na2SiO3・10H2O)]をラジウム温泉水に溶解し、同様に溶解したアラゴナイト由来カルシウムおよびマグネシウム(例えば金属マグネシウム)と混合し、煮沸・冷却することによって得られる。 メタケイ酸塩、カルシウムおよびマグネシウムの配合比は、調製する溶液のpH等により適宜調整することができるが、好ましくは、メタケイ酸塩(ケイ素として):カルシウム:マグネシウムの重量比が約1:0.00001~0.0005:0.001~0.010である。 本発明のメタケイ酸塩溶液は、そのままの形態で飲食物、経口製剤等に用いてもよいが、安定性等を考慮すると、濃縮液として使用するのがより好ましい。濃縮液として使用する場合、例えば、メタケイ酸塩溶液を滴下瓶等に収容し、溶液の所定量を飲食物に滴下して摂取することができる。また、使用時に濃縮液を水等により所定の濃度に希釈して摂取してもよい。 本発明のメタケイ酸塩溶液の1日当たりの摂取量は、ケイ素として約1~50mgの範囲、好ましくは約1~20mg、より好ましくは約5~10mgの範囲である。 本発明のメタケイ酸塩溶液を飲食物に用いる場合、飲食物は特に限定されず、一般の飲食物(例えば、ミネラル水、米飯の炊き水、コーヒー、焼酎の割水等)に用いることができる。本発明のメタケイ酸塩溶液の腎機能または糖尿病に対する効果から、例えば、いわゆる健康食品または機能性食品として用いることもできる。 本発明のメタケイ酸塩溶液を腎機能障害の予防剤もしくは改善剤または糖尿病の予防剤もしくは改善剤として用いる場合、その形態は一般に水溶液、油性溶液、懸濁液、エマルション、シロップまたはエリキシルの形態である。これらの経口液剤は、一般に使用される懸濁剤、乳化剤、非水剤、防腐剤、着色剤、芳香剤等の添加剤を含有してもよい。添加剤の例としては、アーモンドオイル、エチルアルコール、ココナツオイル分画、ゼラチン、グルコースシロップ、グリセリン、水素化食用油、レシチン、メチルセルロース、メチル又はプロピルパラ−ヒドロキシベンゾエート、プロピレングリコール、ソルビトール、ソルビン酸等が挙げられる。 本発明のメタケイ酸塩溶液は、液剤に限らず、錠剤やカプセルに添加して用いてもよい。錠剤及びカプセルは、メタケイ酸塩溶液に加えて、結合剤(例えば、アカシアガム、ゼラチン、ポリビニルピロリドン、ソルビトール、又はトラガカントゴム等)、増量剤(例えば、リン酸カルシウム、グリシン、ラクトース、トウモロコシ澱粉、ソルビトール、サッカロース等)、潤滑剤(例えば、ステアリン酸マグネシウム、ポリエチレングリコール、シリカ、タルク等)、崩壊剤(例えば、ポテト澱粉)、香料、着色剤、湿潤剤等を含有することができる。 以下、本発明を実施例によりさらに詳細に説明するが、本発明は、これらの実施例に限定されるものではない。実施例1(1)水溶性メタケイ酸塩の調製 ケイ素として40.7mg/Lの水溶性メタケイ酸塩、およびpH調製剤[アラゴナイト由来カルシウム(アラゴマリーン;(株)ガイヤテック製)およびマグネシウム(金属マグネシウム;日本重化学工業(株)製)]をラジウム温泉水に加え、pHを11に調整して、水溶性メタケイ酸塩を含むミネラル濃縮水(以下、単に「ミネラル濃縮水」と記す。)を調製した。水溶性メタケイ酸塩は、シリポリ(韓国エスカム社製)を用いた。水溶性メタケイ酸塩溶液の組成を表1に示す。 本実験では、調製したミネラル濃縮水を、2%(v/v)、5%(v/v)の割合で水道水に混ぜたものを被検物質とした。(2)評価試験動物: 試験には、糖代謝異常マウス(KK/Ta jcl)の雄を1群当たり15匹、総数45匹を使用した。KK/Taマウスは、空腹時高血糖・耐糖能異常・高インスリン血症・肥満・高脂血症等を呈するII型糖尿病モデルマウスである。また近年では、遺伝子チップを用いた解析により、肝臓,骨格筋においてM−cadherinの強発現が確認され、さらに、このM−cadherinの遺伝子多型(SNP)と血清トリグリセリド・血清インスリン・耐糖能・体重と有意な相関があることが報告され、II型糖尿病およびメタボリックシンドロームモデルとしての有用性を再認識されるようになっている。 すべての動物は、日本クレア株式会社より4週齢で購入し、検疫・馴化期間を経て、5週齢より実験に用いた。実験条件: マウスの飼育管理および実験は、鹿児島大学フロンティアサイエンス研究推進センター動物実験施設の飼育室に設置しているクリンラック内で行った。その際の室内環境は、温度22±1℃、湿度55±10%、換気回数12回、照明時間は12時間と設定し、通常飼料(CE−2,日本クレア株式会社製)および高脂肪飼料(HFD32,日本クレア株式会社製)、水道水(コントロール群)またはミネラル濃縮水(被験群)は自由摂取とした。評価デザイン KK/Taマウスを表2に示す3群に分け、各群とも25週齢までは通常飼料を、以降は高脂肪飼料にて飼育し、その間に水道水(コントロール群)またはミネラル濃縮水(2%摂取群,5%摂取群)を与え、実験を行った。一般状態および生死、体重、摂餌・摂水量変化: すべての動物について、週に1度、一般状態および生死を目視観察するとともに、電子天秤(AND GF−3000)を用いて体重、摂餌・摂水量を測定した。臓器重量比: 32週齢で、すべてのマウスをペントバルビタール麻酔下での放血によって安楽死させ、各臓器重量(心臓、肝臓、腎臓、脾臓、膵臓、精巣上体周囲脂肪組織)を測定した。血液生化学検査: 試験開始25週間後(30週齢時)、各群より無作為に各10匹を選出し、血液生化学検査に供した。対象マウスより血液を採取し、サンプルを輸送後、株式会社エスアールエルにて検査を行った。 検査は、中性脂肪量、総コレステロール量およびHDLコレステロール量の3項目について行った。これらの測定項目については、採食時に行った。血糖値については、32週齢時に、尾部静脈または眼窩静脈より採血し、簡易血糖測定システム アキュッチェックコンパクト(ロシュ・ダイアグノスティックス株式会社製)を使って測定した。尿糖の測定: 尿糖は、すべての動物について、30週齢で採食時にハイテスパーG(栄研化学株式会社)を用いて測定した。統計処理: 各変数は平均値±標準偏差で示し、Statcel2(有限会社オーエムエス出版製)を用いて、正規性の検定後、以下に示す統計処理を行った。 各群の体重変化(g)については、重複測定-分散分析法により個体間変動および実験個体変動、個体内変動、交互作用変動、誤差変動を解析した。また、臓器重量比(%)については、正規性およびバーレット検定後、分散が均一とみなせる場合はOne−factor ANOVAによって、分散が不均一である場合はクラスカル・ワーリス検定によって、ミネラル濃縮水投与の影響を検定した。これらの検定で、ミネラル濃縮水の影響が確認された場合は、Scheffe’s F 検定によって、コントロール群と2%摂取群、あるいは5%摂取群との比較検定を行って、有意差があるか否かを解析した。 採食時血糖値(mg/dL)および尿糖(−)については、正規性およびバーレット検定後、クラスカル・ワーリス検定によって、ミネラル濃縮水投与の影響を検定し、各群の有意差検定にはScheffe’s F 検定を用いた。 その他の血液生化学変数、中性脂肪量(mg/dL)および総コレステロール量(mg/dL)およびHDLコレステロール量(mg/dL)については、正規性の検定後、One−factor ANOVAによってミネラル濃縮水投与の影響を検定した。結果:1.一般状態および生死、体重、摂餌・摂水量の変化 各群における試験中の体重変化を、図2.1に示し、飼育期間における飼育ケージ毎の摂餌量の変化を図2.2に、摂水量を図2.3に示す。すべての測定値を元に、統計処理を行った結果、実験個体変動および個体内変動ともにp値が0.05よりも大きいため、ミネラル濃縮水の投与量および投与期間による体重差はないといえる。 剖検時の所見として、各群ともに肝臓の白色化が確認され(図1.4中、矢頭)、内臓脂肪が蓄積していることが確認された。同様に、精巣上体周囲にも高度に脂肪が蓄積しており(図中、矢印)、内臓脂肪型メタボリックシンドロームが誘導できていると推測される。剖検所見から2~5%(v/v)の濃度域においては少なくとも急性毒性はないといえる。2.臓器重量比 各臓器の臓器重量比(%)は、臓器重量(g)/体重(g)×100により求めた。また、各臓器ごとの比較を以下(図3.1~3.6)に示す。2.1.心臓 心臓の臓器重量比を、図3.1に示す。各群の数値は、コントロール群で0.36±0.04%(n=16)、2%摂取群で0.36±0.02%(n=15)、5%摂取群で0.36±0.02%(n=14)であった。統計解析の結果、ミネラル濃縮水投与による心臓-臓器重量比の変化は確認できなかった(p>0.05)。2.2.肝臓 同様に、肝臓/臓器重量比(図3.2)はコントロール群で5.20±1.06%(n=16)、2%摂取群で5.34±1.09%(n=15)、5%摂取群で5.35±1.36%(n=14)であった。2.3.腎臓 腎臓/臓器重量比(図3.3,左腎:a,右腎:b)は、コントロール群で左腎0.51±0.04%、右腎0.52±0.05%(n=16)、2%摂取群で左腎0.51±0.06%、右腎0.52±0.06%(n=15)、5%摂取群で左腎0.55±0.06%、右腎0.55±0.06%(n=14)であり、統計解析の結果、ミネラル濃縮水摂取の影響は見られなかった(p>0.05)。2.4.膵臓 膵臓/臓器重量比(図3.4)については、コントロール群0.46±0.09%(n=16)、2%摂取群0.45±0.07%(n=15)、5%摂取群0.39±0.06%(n=14)であり、統計解析の結果、ミネラル濃縮水摂取による臓器重量比変化が認められた(p<0.05)。 しかし、Scheffe’s F 検定による有意差検定では、コントロール群と2%摂取群間、コントロール群と5%摂取群間、および2%摂取群と5%摂取群間ともに有意な差はなかった。2.5.脾臓 脾臓/臓器重量比は、コントロール群0.35±0.12%(n=16)、2%摂取群0.35±0.07%(n=15)、5%摂取群0.32±0.07%(n=14)で、ミネラル濃縮水摂取の影響は確認できなかった(p>0.05)。2.6.精巣上体周囲脂肪組織 高脂肪飼料摂取により、KK/Ta雄マウスの精巣上体周囲には高度に内蔵脂肪が蓄積しており、体重に占める割合がコントロール群で2.73±0.39%(n=6)にまでも上昇している。この内臓脂肪に対するミネラル濃縮水の影響は、2%摂取群で3.29±0.50%(n=5)、5%摂取群で3.57±0.68%(n=4)と、統計解析の結果、影響は確認できなかった(p>0.05)。3.血液生化学検査 次に、血液生化学的データにおける、メタケイ酸塩を含むミネラル濃縮水の影響を調べた。各指標について、以下に述べる。3.1.採食時血糖値 各群の採食時血糖値(図4.1)は、コントロール群で139.4±44.39 mg/dL(n=10)、227.4±76.90mg/dL(n=10)、119.5±31.32mg/dL(n=10)であった。 統計解析の結果、コントロール群と2%摂取群間、および2%摂取群と5%摂取群間で有意な差があった(p<0.01)。3.2.中性脂肪量 各群の中性脂肪量(図4.2)は、コントロール群で273.7±143.43mg/dL(n=10)、2%摂取群で307.1±188.56mg/dL(n=10)、299.1±191.92mg/dL(n=10)であり、各群間に有意な差はなかった(p>0.05)。3.3.総コレステロール量 総コレステロール量(図4.3)については、コントロール群で182.7±26.71mg/dL(n=10)、2%摂取群で163.0±23.65mg/dL(n=10)、5%摂取群で185.1±24.63mg/dL(n=10)であった。統計解析の結果、血中の総コレステロール量へのミネラル濃縮水の影響は確認されなかった(p>0.05)。3.4.HDLコレステロール量 各群における血中HDLコレステロール量(図4.4)は、コントロール群で100.33±13.54 mg/dL(n=9)、2%摂取群で92.9±12.33mg/dL(n=10)、5%摂取群で101.2±11.74mg/dL(n=10)であり、統計解析の結果、ミネラル濃縮水のHDLコレステロール量への影響は見当たらなかった(p>0.05)。4.尿糖測定 尿糖(−)は、−を0、+を1、++を2、+++を3としてスコアし、30週齢時の測定データを統計解析に利用した。その結果、コントロール群では2.3±0.82(n=10)、2%摂取群では1.0±1.05(n=10)、5%摂取群では0.9±1.20(n=10)であった。多重比較検定による各群間の差は、コントロール群と2%摂取群(p<0.05)、コントロール群と5%摂取群(p<0.05)の間で有意な差が検出されているが、2%摂取群と5%摂取群の間では有意な差は見られなかった(p>0.05)。 尿糖測定の結果(図5.1)を見ると、ミネラル濃縮水の投与によって、有意に尿糖の検出が少なくなっている。このことは、メタケイ酸塩を含むミネラル濃縮水が腎臓での糖の再吸収を向上させている可能性が示唆される。本発明のメタケイ酸塩溶液の走査電子顕微鏡(SEM)写真である。従来技術のメタケイ酸塩溶液の走査電子顕微鏡(SEM)写真である。各群における試験中の体重変化を示すグラフである。飼育期間中の飼育ゲージ毎の摂餌量の変化を示すグラフである。飼育期間中の飼育ゲージ毎の摂水量の変化を示すグラフである。各群(a.コントロール群、b.2%摂取群、c.5%摂取群)の剖検写真である。各群の心臓/臓器重量比(%)を示すグラフである。各群の肝臓/臓器重量比(%)を示すグラフである。各群の腎臓/臓器重量比(%)を示すグラフである。各群の膵臓/臓器重量比(%)を示すグラフである。各群の脾臓/臓器重量比(%)を示すグラフである。各群の精巣上体周囲脂肪組織/臓器重量比(%)を示すグラフである。各群の血糖値(mg/dL)を示すグラフである。各群の中性脂肪量(mg/dL)を示すグラフである。各群の総コレステロール量(mg/dL)を示すグラフである。各群のHDLコレステロール量(mg/dL)を示すグラフである。各群の尿糖の測定結果を示すグラフである。 水溶性のメタケイ酸塩および水を含有し、pHが8~12である、メタケイ酸塩溶液であって、ケイ素酸化鉱物を焼成し、ガス化した後に回収して得られるメタケイ酸塩を水に溶解し、カルシウムおよびマグネシウムと混合し、煮沸、冷却することにより得られる多孔性球状コロイドを形成してなる、前記メタケイ酸塩溶液。 ケイ素酸化鉱物由来のメタケイ酸塩、カルシウムまたはカルシウム塩、およびマグネシウムを含有する複合水溶液から得られる、請求項1に記載のメタケイ酸塩溶液。 メタケイ酸塩をケイ素として10~1000mg/L含有する、請求項1または2に記載のメタケイ酸塩溶液。メタケイ酸塩をケイ素として500~1000mg/L含有する、請求項1または2に記載のメタケイ酸塩溶液。メタケイ酸塩をケイ素として10~100mg/L含有する、請求項1または2に記載のメタケイ酸塩溶液。pHが10~12である、請求項4に記載のメタケイ酸塩溶液。pHが8~9である、請求項5に記載のメタケイ酸塩溶液。請求項1~7のいずれかに記載のメタケイ酸塩溶液を含有する、飲食物。 ミネラル水である、請求項8に記載の飲食物。 請求項1~7のいずれかに記載のメタケイ酸塩溶液を含有する、糖尿病の予防剤または改善剤。
 ソマチットは、フランスの生物物理学者「
ソマチットは、フランスの生物物理学者「